La indicación para la resección de metástasis es una decisión individual que debe tomarse de manera interdisciplinaria junto con el paciente. En este contexto, la resección curativa R0 representa el estándar de oro de las posibilidades terapéuticas. También el orden de las medidas quirúrgicas en caso de metástasis sincrónica debe decidirse de forma individual.
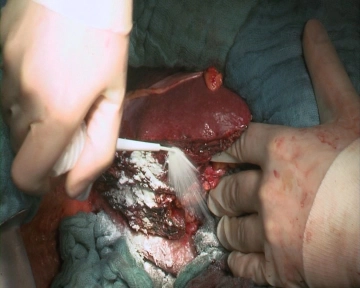
En el caso demostrado, existía la sospecha de una recidiva de metástasis hepáticas en el segmento VI después de una resección de metástasis hepáticas 5 meses antes.
Las técnicas que preservan el parénquima se prefieren en la cirugía de metástasis. Las resecciones limitadas o atípicas son preferibles a las anatómicas, ya que queda más parénquima hepático, lo que es especialmente relevante en situaciones de recidiva. Las resecciones con gran pérdida de parénquima no pueden aumentar la seguridad oncológica ni la prognosis a largo plazo.
No es el ancho, sino la ausencia de tumor en el margen de resección lo que es decisivo para evitar una recidiva. Incluso una resección R1 presunta es aceptable en casos excepcionales, porque a través de la técnica de resección (aspiración/electrocoagulación del tejido hepático), a pesar de tejido tumoral detectable microscópicamente en el borde del preparado, el margen de resección en el paciente puede estar libre de tumor.
En situaciones de recidiva, la extensión de la resección y la forma de resección (atípica, anatómica) dependen de la localización y la extensión de la primera operación. En particular, debe tenerse en cuenta la anatomía vascular intrahepática alterada por la primera intervención.
A pesar de una buena imagen de corte, la diferenciación entre una lesión hepática benigna y maligna puede ser difícil.
La afectación bilobar, la manifestación tumoral extrahepática o la infiltración de vasos mayores ya no se consideran contraindicaciones. La estrategia de tratamiento óptima resulta de la extensión o del número de tumores/metástasis a operar.
En resecciones mayores (metástasis múltiples), debe calcularse el parénquima hepático restante. Lo decisivo es el volumen hepático restante después de la resección („future remnant liver volume“ = FRLV) y las estructuras vasculares necesarias para ello. Este debería ser al menos del 30% del hígado restante, pero debe calcularse considerablemente más alto en caso de hígado previamente dañado (quimioterapia, cirrosis hepática).
Si es probable que se infrinjan estos valores mediante la resección planificada, debe evaluarse la posibilidad de un acondicionamiento preoperatorio.
- Inducción de hipertrofia preop. (p. ej., PVE = embolización de la vena porta)
- División in situ/ALPPS (Associating Liver Partition and Portal vein ligation for Staged hepatectomy)
- Resecciones en 2 o más tiempos
- Combinación con procedimientos ablativos (p. ej., RFA = ablación por radiofrecuencia)
- Resección quirúrgica secundaria después de quimioterapia neoadyuvante
Mediante la combinación de métodos quirúrgicos e intervencionistas, posiblemente con terapia sistémica, incluso hallazgos muy avanzados pueden llevarse a una resección potencialmente curativa.
Las metástasis primariamente no resecables pueden convertirse de un estadio paliativo a uno curativo mediante quimioterapia. En este caso, debe operarse tan pronto como se alcance la resecabilidad, para mantener la toxicidad de los medicamentos lo más baja posible y para reducir el problema de la localización dificultada por la regresión tumoral.
La resección simultánea con el tumor primario en metástasis sincrónicas debe intentarse en focos bien accesibles. El postulado de realizar la resección de la(s) metástasis hepática(s) en principio después de 2-3 meses no puede mantenerse así.